
Por que a escolha do biorreator impacta diretamente sua pesquisa
A escolha de um biorreator não é apenas técnica — é estratégica.
Ela influencia diretamente a confiabilidade dos dados, a reprodutibilidade dos experimentos e a viabilidade de escala do seu processo.
Um equipamento desalinhado pode gerar:
- perda de amostras
- inconsistência de resultados
- retrabalho experimental
- atrasos no cronograma
O que considerar antes de escolher um biorreator
Definição da aplicação
1. Cultura Celular (Células de Mamíferos ou Insetos)
Neste cenário, o desafio central é a fragilidade mecânica. Diferente de bactérias, essas células não possuem parede celular rígida, o que as torna extremamente sensíveis ao estresse de cisalhamento (shear stress).
-
Controle de Agitação: Exige o uso de impelidores de baixo impacto (como o tipo Marine ou Pitched Blade) para garantir a mistura sem romper as membranas celulares.
-
Aeração e Espargimento: O fornecimento de O² deve ser delicado. Bolhas grandes podem causar danos ao eclodirem na superfície; por isso, utiliza-se microespargidores e, muitas vezes, o controle preciso de O² para manutenção do pH citoplasmático.
-
Complexidade Nutricional: Requer meios de cultura complexos e controle rigoroso de temperatura (geralmente 37°C) e metabólitos para evitar a toxicidade por amônia ou lactato.
2. Fermentação Microbiana (Bactérias, Fungos e Leveduras)
Aqui, o foco muda para a alta demanda metabólica e a velocidade de crescimento. Microrganismos costumam ser robustos, mas consomem oxigênio e nutrientes em taxas altíssimas.
-
Transferência de Massa: Devido à alta densidade celular, o equipamento precisa de uma capacidade de transferência de oxigênio superior. Isso implica em agitação vigorosa (impelidores tipo Rushton) e altas taxas de aeração.
-
Gerenciamento Térmico: Processos fermentativos são fortemente exotérmicos. O sistema de resfriamento (jaqueta ou serpentina) deve ser altamente eficiente para dissipar o calor gerado pelo metabolismo acelerado.
-
Cinética de Crescimento: O controle deve ser capaz de acompanhar mudanças rápidas de pH e demanda de nutrientes em janelas de tempo curtas.
3. Produção de Biomoléculas (Proteínas Recombinantes, Vacinas e Enzimas)
Quando o objetivo não é apenas "crescer células", mas sim fazê-las "fabricar" um produto, o critério de controle torna-se ainda mais analítico.
-
Estratégias de Alimentação (Feeding): O processo geralmente exige a transição de uma fase de crescimento para uma fase de indução. O biorreator deve permitir estratégias de fed-batch (batelada alimentada) precisas para maximizar o rendimento.
-
Estabilidade do Produto: Muitas biomoléculas são termolábeis ou sensíveis a proteases. O controle pós-indução pode exigir a redução da temperatura ou ajustes finos de pH para garantir a integridade da proteína expressa.
-
Monitoramento de Pureza e Escalonamento: A reprodutibilidade é a palavra-chave. Sensores de oxigênio dissolvido (O²) e potencial redox tornam-se ferramentas essenciais para garantir que cada lote mantenha o mesmo perfil de expressão proteica.

Escala do processo
1. Escala de Bancada (Desenvolvimento e Triagem)
O objetivo aqui é a agilidade e a descoberta. É o estágio onde se testam as variáveis e se define a "receita" do processo.
-
Foco Técnico: Otimização de meios de cultura, seleção de linhagens e testes de parâmetros (pH, Temperatura, O²).
-
Flexibilidade: Equipamentos de bancada (geralmente de 0,5 a 10 litros) devem ser fáceis de montar, esterilizar (muitas vezes via autoclave) e permitir mudanças rápidas de configuração.
-
Coleta de Dados: É a fase de gerar o máximo de informação com o mínimo de custo por ensaio.
2. Escala Piloto (Validação e Prova de Conceito)
Este é o "purgatório" dos projetos: onde a maioria falha. O objetivo é provar que o que funcionou na bancada se mantém estável em volumes maiores (50 a 500 litros).
-
Foco Técnico: Estudo da transferência de massa e calor. O que era fácil de resfriar em 2 litros torna-se um desafio de engenharia em 200 litros.
-
Simulação do Real: Aqui já se utilizam sistemas de automação e controle idênticos aos industriais. É onde se ajustam os cálculos de kLa (coeficiente de transferência de oxigênio) para garantir que as células não sofram com a falta de ar no centro do tanque.
-
Gargalos: Identificação de problemas de logística, como o tempo de esterilização e o preparo de grandes volumes de meio.
3. Escala Industrial (Produção e Viabilidade Econômica)
Aqui o foco é eficiência, repetibilidade e custo. O biorreator deixa de ser um instrumento de laboratório e passa a ser uma unidade de fábrica (1.000 litros ou mais).
-
Foco Técnico: Robustez operacional e automação total (Sistemas CIP/SIP - Cleaning/Sterilization in Place). O equipamento precisa rodar 24/7 com o mínimo de intervenção humana.
-
Economia de Processo: Pequenas variações no rendimento aqui significam prejuízos enormes. O controle de precisão serve para garantir que o lote de hoje seja idêntico ao de ontem.
-
Conformidade: Rigor total com normas regulatórias (como a GMP), exigindo sensores com calibração rastreável e registro de dados invioláveis.
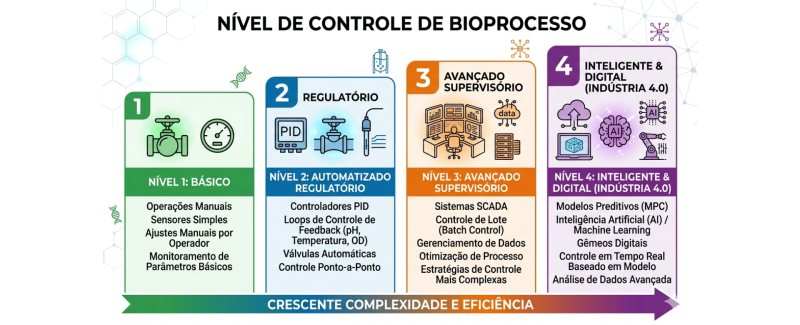
Nível de controle de bioprocesso
1. pH (Potencial Hidrogeniônico)
O pH é o indicador da "saúde" do meio. Em bioprocessos, ele flutua conforme as células consomem nutrientes e liberam metabólitos (como lactato ou O²).
-
Aprofundamento: Um controle rigoroso não usa apenas bombas de ácido/base. Em culturas de mamíferos, o controle é feito via injeção de CO², que reage com o bicarbonato do meio para manter o equilíbrio de forma mais suave, evitando "choques" químicos que poderiam matar as células.
-
Impacto: Fora da faixa ideal, as proteínas podem desnaturar ou a célula pode entrar em apoptose (morte programada).
2. Oxigênio Dissolvido (DO - Dissolved Oxygen)
É o parâmetro mais dinâmico e difícil de controlar em escala.
-
Aprofundamento: O controle moderno trabalha com cascatas de oxigenação. Quando o nível de O² cai, o biorreator primeiro aumenta a agitação; se não for suficiente, aumenta o fluxo de ar; por último, injeta O² puro. Isso economiza recursos e evita o estresse mecânico desnecessário.
-
Impacto: A falta de O² (hipóxia) altera a rota metabólica, forçando a célula a produzir subprodutos indesejados (como álcool ou ácidos), o que reduz drasticamente a produtividade.
3. Temperatura
Parece o mais simples, mas é o que exige maior estabilidade térmica.
-
Aprofundamento: Em biorreatores de precisão, utiliza-se o controle PID (Proporcional-Integral-Derivado) ligado a uma jaqueta de aquecimento/resfriamento. Isso evita a "overshoot" (quando a temperatura passa do ponto e precisa voltar), garantindo que a oscilação seja menor que 0,1°C.
-
Impacto: A temperatura dita a velocidade das reações enzimáticas. Mesmo 1°C acima do ideal pode inibir o crescimento ou alterar a estrutura da biomolécula final.
4. Agitação
Sua função vai muito além de "mexer o caldo"; ela garante a homogeneidade.
-
Aprofundamento: O foco aqui é o equilíbrio entre mistura e cisalhamento. Uma agitação eficiente deve garantir que o oxigênio e os nutrientes cheguem a cada célula, mas sem romper a membrana celular. Em processos sensíveis, a geometria das pás (impelidores) é desenhada para criar um fluxo axial suave, em vez de um turbilhão agressivo.
-
Impacto: Uma agitação ruim cria "zonas mortas" no tanque, onde o pH e a temperatura ficam fora do controle, gerando um lote heterogêneo e imprevisível.

Tipos de biorreatores e suas aplicações
Biorreatores de bancada
O Impacto da Escala no Projeto
A escolha do equipamento deve considerar o momento da pesquisa. Ignorar essa progressão pode comprometer o projeto, já que a escala muda completamente o resultado esperado:
1. Bancada (Desenvolvimento e P&D)
Ideal para as fases iniciais, onde a agilidade e a descoberta são prioridades:
-
Maior Flexibilidade: O equipamento se adapta ao pesquisador. A modularidade permite trocar vasos (vidro ou single-use) e impelidores rapidamente. Sendo multiprocesso, o mesmo controlador pode gerenciar diferentes culturas apenas ajustando o software.
-
Menor Custo Inicial: Minimiza riscos. Volumes de 1 a 5 litros consomem muito menos insumos e não exigem infraestrutura industrial complexa. Além disso, garante segurança financeira: errar em 2 litros é um aprendizado; em 2.000 litros é um desastre.
-
Testes de Parâmetros: É o "cérebro" do escalonamento. Permite a varredura de variáveis para encontrar o ponto ideal de produtividade e a caracterização de kLa com sensores de alta precisão, gerando dados robustos para validar o futuro scale-up.
2. Piloto (Validação)
Fase para estudar a transferência de massa e calor em volumes maiores, preparando o processo para o ambiente fabril.
3. Industrial (Produção)
Foco total em eficiência, repetibilidade e conformidade regulatória (GMP) em larga escala.

Critérios técnicos que evitam erros na escolha
Capacidade de escalonamento
A Replicabilidade e o Desafio da Transição de Escala (Scale-up)
O equipamento não deve apenas permitir diferentes volumes, ele deve garantir a similaridade de processos. Sem essa capacidade, o pesquisador enfrenta o chamado "vácuo de escalonamento", onde o rendimento cai drasticamente ao aumentar o tamanho do tanque.
Como o equipamento garante essa replicação?
-
Similaridade Geométrica: Os biorreatores de uma mesma linha devem manter as proporções entre o diâmetro do vaso e a altura do líquido, além do design dos impelidores. Isso garante que o padrão de fluxo (como o fluido se move) seja constante, independentemente do volume.
-
Correlação de Parâmetros de Engenharia: O sistema de controle deve permitir que você replique critérios específicos, como:
-
Potência por Volume (PIV): Manter a mesma energia de agitação distribuída no meio.
-
Velocidade de Ponta do Impelidor (Tip Speed): Crucial para processos sensíveis ao cisalhamento.
-
kLa Constante: Garantir que a taxa de transferência de oxigênio para as células seja a mesma na bancada e na indústria.
-
-
Instrumentação e Automação Padronizada: Utilizar a mesma família de sensores e o mesmo software de controle em diferentes escalas facilita a migração de dados. As "curvas de processo" validadas no pequeno volume podem ser carregadas como diretrizes para o volume maior, reduzindo o tempo de setup.
-
Modelagem de Processo: Equipamentos modernos permitem simular o comportamento do fluido antes mesmo de iniciar a produção, identificando antecipadamente "zonas mortas" ou gradientes de temperatura que só apareceriam em grandes tanques.
Por que isso é um redutor de riscos?
A transição de escala é, por natureza, um risco financeiro e biológico. Se o equipamento permite replicar condições fielmente, você elimina variáveis incertas. Isso significa que o comportamento celular observado na bancada será previsível na escala industrial, garantindo que o produto final (seja uma proteína, vacina ou biomassa) mantenha a mesma pureza e concentração.
Sistema de monitoramento e automação
A escolha do equipamento deve passar por uma avaliação rigorosa da camada de inteligência e controle. Sem esses pilares, a reprodutibilidade do bioprocesso fica seriamente comprometida:
1. Controle Automatizado (Reprodutibilidade e Segurança)
A automação vai além de manter o pH ou a temperatura estáveis; ela garante a integridade do lote.
-
Malhas de Controle PID: O sistema deve atuar de forma preditiva para evitar oscilações bruscas. Por exemplo, ao detectar uma queda no oxigênio, o sistema aumenta a agitação automaticamente antes de injetar O² puro.
-
Alarmes e Segurança: Um controle automatizado eficiente monitora pressões e níveis de espuma, interrompendo o processo ou enviando alertas em caso de desvios, protegendo o investimento e as células.
2. Registro de Dados Confiável (Rastreabilidade e Ciência)
Dados são o ativo mais valioso de um bioprocesso. Se não foi registrado, o experimento "não aconteceu".
-
Historiadores de Dados: O equipamento deve registrar cada variável em intervalos de segundos, criando um "RG" completo de cada lote (o Batch Record).
-
Conformidade com Normas (CFR Part 11): Para aplicações farmacêuticas, os registros devem ser invioláveis, com trilhas de auditoria (audit trail) que mostram quem alterou qualquer parâmetro e quando isso foi feito.
3. Integração com Softwares (Ecossistema de Dados)
O biorreator não deve ser uma "ilha"; ele precisa se comunicar com o restante do ecossistema técnico.
-
Conectividade e Exportação: Possibilidade de exportar dados para ferramentas de análise estatística ou integração direta com sistemas LIMS (Gestão de Laboratório) e SCADA (Supervisão Industrial).
-
Acesso Remoto: Softwares modernos permitem que o pesquisador monitore o biorreator em tempo real via nuvem ou rede local, essencial para processos de longa duração que exigem vigilância constante.

Facilidade de operação
Operação e Manutenção: A Eficiência no Dia a Dia
A tecnologia de um biorreator deve servir para simplificar a ciência, não para criar barreiras. Equipamentos complexos demais ou com suporte deficiente reduzem a eficiência produtiva da equipe.
1. Interface Intuitiva (Foco no Pesquisador)
Um sistema de controle amigável reduz drasticamente a curva de aprendizado e a incidência de erros operacionais.
-
Visualização em Tempo Real: Telas que exibem gráficos de tendência e o status de todas as bombas e válvulas de forma clara permitem intervenções rápidas.
-
Configuração de Receitas: A facilidade em programar e salvar "receitas" de processo garante que diferentes pesquisadores operem o equipamento com o mesmo padrão de qualidade.
2. Facilidade de Limpeza e Esterilização (Integridade do Processo)
Em bioprocessos, a contaminação é o maior inimigo. O design do equipamento deve facilitar a assepsia total.
-
Acessibilidade: Vasos e componentes devem ser fáceis de desmontar e limpar, sem "pontos mortos" onde resíduos possam se acumular.
-
Autoclavagem e Vedação: Sensores e selos mecânicos devem ser robustos o suficiente para suportar ciclos repetidos de esterilização sem perder a calibração ou a integridade.
3. Suporte Técnico (Continuidade Operacional)
Biorreatores são equipamentos de longo prazo. O suporte técnico é o que garante que seu investimento não se torne obsoleto ou fique parado por falta de peças.
-
Disponibilidade de Peças: Ter acesso rápido a consumíveis (como mangueiras, filtros e reparos de sensores) é vital para não interromper cronogramas de pesquisa.
-
Especialização Local: Contar com uma equipe técnica que entende as particularidades da biotecnologia brasileira facilita a calibração e a manutenção preventiva, evitando que o equipamento pare no meio de um lote crítico.
Erros mais comuns ao escolher um biorreator
Escolher um biorreator baseando-se apenas em critérios superficiais é um dos caminhos mais rápidos para comprometer a viabilidade de um projeto biotecnológico. Fique atento a estes quatro pontos críticos:
1. Priorizar Preço em vez de Aplicação
O biorreator mais barato raramente é o mais econômico a longo prazo. Um equipamento que não oferece o tipo de agitação ideal ou a sensibilidade de gases necessária para a sua célula resultará em baixa produtividade e perda de lotes. O investimento deve ser pautado na especificidade técnica do seu processo (seja cultura celular ou fermentação), garantindo que o hardware suporte a biologia.
2. Ignorar a Necessidade Futura de Escala
Muitos projetos morrem na transição do laboratório para a fábrica porque foram desenvolvidos em sistemas que não permitem a replicabilidade de condições. Adquirir um equipamento de bancada sem considerar se ele possui similaridade geométrica e de controle com as escalas piloto e industrial é criar um "vácuo de escalonamento". Lembre-se: em bioprocessos, a escala muda completamente o resultado se não houver planejamento desde o dia um.
3. Subestimar o Controle de Bioprocesso
Achar que um controle básico de "liga/desliga" é suficiente para processos sensíveis é um erro grave. A falta de precisão em malhas de controle (como o PID para temperatura e pH) ou a ausência de uma cascata inteligente para oxigênio dissolvido gera instabilidade metabólica. Sem um controle rigoroso, você perde a previsibilidade, tornando cada lote uma surpresa cara.
4. Não Avaliar o Suporte Técnico
Um biorreator parado por falta de uma peça de reposição ou por dificuldade de calibração interrompe cronogramas inteiros de pesquisa e produção. Ignorar a presença e a agilidade do suporte técnico do fabricante — especialmente em componentes críticos como sensores e sistemas de vedação — é colocar o projeto em risco. A proximidade com o suporte especializado garante que o biorreator, que não é tudo igual, opere sempre em sua máxima performance.

Na prática, como escolher o Biorreator ideal?
A decisão correta não é apenas uma compra técnica, mas um alinhamento estratégico que depende de três fatores fundamentais.
1. Objetivo da Pesquisa
O ponto de partida deve ser a biologia do processo. Você está buscando a expressão de uma proteína específica, o crescimento de biomassa ou a produção de um metabólito secundário?
-
Aprofundamento: Para triagem e otimização de meios, a flexibilidade da escala de bancada é imbatível. Já para a produção de lotes para testes clínicos, o foco muda para a robustez e repetibilidade. Escolher sem alinhar ao objetivo final é o motivo pelo qual, muitas vezes, um biorreator parece igual, mas não funciona igual.
2. Nível de Controle Necessário
Quanto mais sensível for o seu microrganismo ou célula, maior deve ser o rigor da instrumentação.
-
Aprofundamento: Avalie se o processo exige controles básicos ou cascatas complexas (como agitação vinculada ao O dissolvido). Em processos de alta densidade, o controle manual é impossível; a automação e o registro de dados tornam-se ativos estratégicos para garantir que cada lote seja idêntico ao anterior. Afinal, o que garante resultados confiáveis em um biorreator não é apenas o hardware, mas a precisão do controle de bioprocesso. Lembre-se: um biorreator não é tudo igual justamente pela sua capacidade de resposta a essas variáveis.
3. Possibilidade de Crescimento do Processo (Escalabilidade)
Um erro comum é comprar um equipamento que atende ao "hoje", mas bloqueia o "amanhã".
-
Aprofundamento: Se existe a intenção de levar o produto ao mercado, o equipamento de bancada deve ser o espelho tecnológico da escala industrial. Isso significa ter a mesma geometria, o mesmo tipo de impelidor e a mesma lógica de software. Sem essa visão de futuro, a transição de escala torna-se um risco técnico altíssimo, pois a escala muda completamente o resultado se não houver planejamento desde o início.
Conclusão: escolher certo é evitar retrabalho
O biorreator ideal não é necessariamente o mais avançado ou o mais caro do mercado. É aquele que atende sua aplicação com precisão técnica, permite a evolução do projeto e, acima de tudo, garante consistência nos resultados. Ao alinhar esses três pilares, você transforma um investimento em equipamento em uma vantagem competitiva de longo prazo.

