
Controle de pH em Biorreatores: O Fator Invisível que Define o Sucesso do Processo
Guia Completo, Estratégias e Otimização Industial
O que é controle de pH em biorreatores?
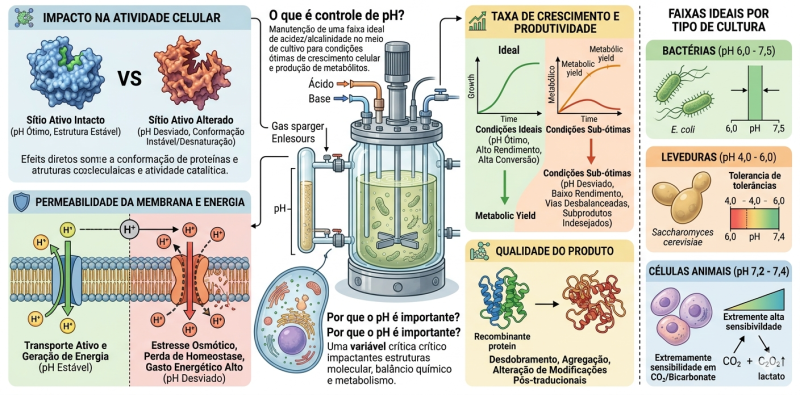
O controle de pH em biorreatores consiste na manutenção de uma faixa ideal de acidez ou alcalinidade dentro do meio de cultivo, garantindo condições ótimas para o crescimento celular e produção de metabólitos. Em processos da Engenharia Bioquímica, esse parâmetro é considerado crítico para desempenho e estabilidade operacional.
Por que o pH é tão importante em processos biotecnológicos?
O pH atua como uma variável crítica porque interfere diretamente em estruturas moleculares, equilíbrio químico e metabolismo celular. Pequenas variações podem deslocar todo o sistema para estados menos eficientes ou até inviáveis. Esse comportamento só pode ser compreendido dentro da lógica de controle de bioprocessos, onde variáveis como pH deixam de ser isoladas e passam a fazer parte de um sistema integrado — inclusive dependendo diretamente do tipo de biorreator, da configuração e da escala do sistema.
Entenda por que isso muda completamente o processo em Biorreator não é tudo igual: tipos, aplicações e por que a escala muda completamente o resultado
Impacto na atividade celular
Afeta diretamente enzimas e proteínas. Enzimas possuem uma faixa ótima de pH onde sua estrutura tridimensional (conformação) é estável. Alterações de pH mudam a ionização dos aminoácidos no sítio ativo, reduzindo ou inibindo a atividade catalítica. Em extremos, ocorre desnaturação proteica irreversível, comprometendo vias metabólicas inteiras.
Exemplo prático: uma única enzima limitante inibida pode reduzir drasticamente a produção global do sistema.
Influencia a permeabilidade da membrana celular
O pH altera o gradiente de prótons (ΔpH), essencial para transporte ativo e geração de energia. Modifica a carga elétrica da membrana, impactando a entrada de nutrientes e saída de metabólitos. Pode causar estresse osmótico e acidificação intracelular, levando a perda de homeostase. Em casos críticos, a célula gasta mais energia tentando se equilibrar do que crescer ou produzir.
Controla a taxa de crescimento microbiano
Cada microrganismo possui uma faixa ótima de pH (ex: bactérias neutrofílicas ~6,5–7,5).
Fora dessa faixa:
• Redução da velocidade de divisão celular
• Alteração na expressão gênica
• Ativação de mecanismos de estresse
Em pH extremos, ocorre inibição total ou morte celular.
O pH também influencia a competição microbiana, favorecendo ou inibindo contaminantes.
Influência na produtividade
• pH fora da faixa ideal reduz rendimento
• Desbalanceia vias metabólicas, desviando energia para manutenção celular.
• Reduz eficiência de conversão de substrato em produto (menor yield).
• Pode limitar etapas críticas da biossíntese (enzimas chave sensíveis ao pH).
Pode gerar subprodutos indesejados
Afeta qualidade do produto final
Proteínas recombinantes podem sofrer:
• Desdobramento (misfolding)
• Agregação
• Alterações em modificações pós-traducionais
• Em fermentações industriais:
• Mudança de sabor/aroma (alimentos)
• Alteração de pureza e atividade (fármacos)
• O pH também impacta a estabilidade do produto ao longo do tempo.
Tratar o pH apenas como um “parâmetro de controle” é uma simplificação perigosa. Na prática, ele é um indicador dinâmico do estado metabólico do sistema. Na prática, quando esse erro acontece, o problema raramente está no pH em si — mas na interpretação do processo como um todo.
Veja como identificar quando o seu processo está falhando aqui
Queda de pH → geralmente associada à produção de ácidos (ex: fermentação)
Aumento de pH → consumo de ácidos ou produção de compostos básicos
Ou seja, controlar pH não é só ajustar com ácido/base, é interpretar o que o sistema está fazendo.
Faixas ideais por tipo de cultura
Essas faixas não são arbitrárias — refletem adaptações evolutivas, estabilidade enzimática e equilíbrio metabólico. Porém, tratá-las como fixas é uma simplificação: o pH ótimo pode variar ao longo do processo (fase de crescimento vs. produção).
Bactérias
Faixa típica: pH 6,0 – 7,5
Por que essa faixa?
- A maioria das bactérias industriais (ex: E. coli, Bacillus) é neutrofílica, com metabolismo otimizado próximo ao pH neutro.
- Enzimas citoplasmáticas funcionam melhor quando o pH externo permite manter o pH intracelular ~7,0–7,5.
O que acontece fora da faixa:
- pH baixo (<6,0):
- Entrada excessiva de prótons → acidificação interna
- Ativação de bombas de efluxo (alto gasto energético)
- Redução da síntese de proteínas
- pH alto (>7,5–8,0):
- Desestabilização de gradientes eletroquímicos
- Prejuízo no transporte de nutrientes
Impacto prático:
- Crescimento rápido ocorre perto do neutro, mas:
- Alguns processos usam pH levemente ácido para reduzir contaminação
- Produção pode exigir ajuste fino:
- Ex: antibióticos ou enzimas podem ter pH ótimo diferente do crescimento
Leveduras
Faixa típica: pH 4,0 – 6,0
Por que essa faixa?
- Leveduras como Saccharomyces cerevisiae são acidotolerantes.
- Conseguem manter pH interno estável mesmo em ambiente ácido.
Vantagens operacionais:
- Menor risco de contaminação bacteriana (bactérias não toleram pH baixo tão bem)
- Melhor estabilidade de certos produtos fermentativos (ex: etanol)
O que acontece fora da faixa:
- pH muito baixo (<4,0):
- Estresse ácido → redução da viabilidade celular
- Alteração no transporte de açúcares
- pH alto (>6,0):
- Aumenta risco de contaminação
- Pode alterar vias metabólicas (menos fermentação, mais respiração)
Impacto prático:
- pH influencia diretamente:
- Produção de etanol vs. biomassa
- Formação de compostos secundários (aroma, ácidos orgânicos)
- Em processos industriais, muitas vezes o pH é mantido propositalmente ácido para controle microbiológico, não apenas performance.
Células animais
Faixa típica: pH 7,2 – 7,4
Por que essa faixa?
- Reflete o ambiente fisiológico (ex: sangue humano ~7,4).
- Extremamente sensíveis a variações → baixa tolerância a desvios.
Características críticas:
- Dependem de sistemas tampão (principalmente bicarbonato/CO₂)
- Pequenas variações (±0,2) já impactam fortemente o metaboliso
O que acontece fora da faixa:
- pH baixo (<7,0):
- Acúmulo de lactato → acidose metabólica
- Redução na síntese de proteínas (ex: anticorpos monoclonais)
- pH alto (>7,6):
- Alteração na estrutura de proteínas secretadas
- Prejuízo na viabilidade celular
Impacto prático:
- Afeta diretamente:
- Glicosilação de proteínas (qualidade de biofármacos)
- Taxa de crescimento e longevidade da cultura
- O pH está fortemente ligado ao controle de:
- CO₂ dissolvido
- Alimentação (feed)
- Produção de metabólitos (lactato, amônia)
Síntese técnica
- Bactérias: equilíbrio entre crescimento rápido e eficiência metabólica
- Leveduras: tolerância ácida como vantagem competitiva
- Células animais: alta sensibilidade → controle extremamente preciso
O pH não define apenas “se a célula cresce”, mas como ela cresce e o que ela produz.
Como o pH varia dentro de um biorreator?
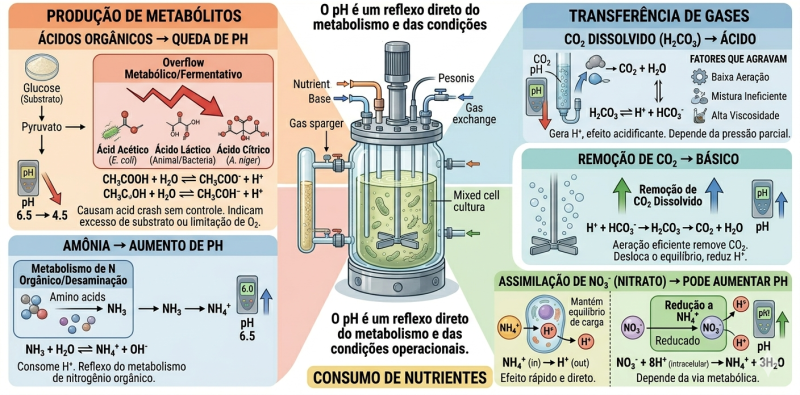
O pH é uma variável dinâmica, resultado do balanço entre produção/consumo de espécies químicas, transferência de massa e capacidade tampão do meio. Não é apenas “algo que muda”, mas um reflexo direto do metabolismo e das condições operacionais.
Produção de metabólitos
- Ácidos orgânicos → reduzem pH
- Durante metabolismo fermentativo ou overflow metabólico, células produzem:
- Ácido acético (E. coli)
- Ácido láctico (células animais e bactérias)
- Ácido cítrico (Aspergillus niger)
- Esses compostos liberam H⁺ no meio, causando queda de pH.
Dinâmica real:
- Inicialmente: crescimento → pH estável ou leve queda
- Alta densidade celular: acúmulo de ácidos → queda acelerada de pH
- Pode ocorrer “acid crash” se não houver controle adequado
Implicações:
- Indica excesso de substrato ou limitação de oxigênio
- Sinal clássico de desbalanceamento metabólico
- Amônia → aumenta pH
- Produzida por:
- Desaminação de aminoácidos
- Metabolismo de nitrogênio orgânico
- Amônia (NH₃) consome H⁺ ao equilibrar com NH₄⁺ → elevação do pH
Transferência de gases
- CO₂ dissolvido → forma ácido carbônico
Quando o CO₂ entra no líquido:
CO₂ + H₂O ⇌ H₂CO₃ ⇌ H⁺ + HCO₃⁻
- Geração de H⁺ → redução do pH
- Quanto maior a pressão parcial de CO₂, maior o efeito acidificante
Fatores que agravam:
- Baixa aeração
- Mistura ineficiente
- Alta viscosidade do meio
- Remoção de CO₂ → aumento do pH
- Aeração eficiente remove CO₂ dissolvido
- Equilíbrio se desloca → redução de H⁺ → pH sobe
Implicações operacionais:
- Ajustes de:
- Taxa de aeração
- Agitação
- Pressão
→ impactam diretamente o pH, mesmo sem adicionar ácido/base
Consumo de nutrientes
- NH₄⁺ (amônio) → acidifica
- Quando células assimilam NH₄⁺:
- Liberam H⁺ no meio para manter equilíbrio de carga
→ queda de pH
Característica importante:
- Efeito rápido e direto
- Muito comum em processos com fonte de nitrogênio amoniacal
- NO₃⁻ (nitrato) → pode alcalinizar
- A assimilação de NO₃⁻ envolve: Redução a NH₄⁺ dentro da célula
- Esse processo consome prótons (H⁺)
→ aumento do pH
Observação crítica:
- Esse efeito depende da via metabólica ativa
- Nem todos os microrganismos utilizam nitrato eficientemente
Interação entre os fatores
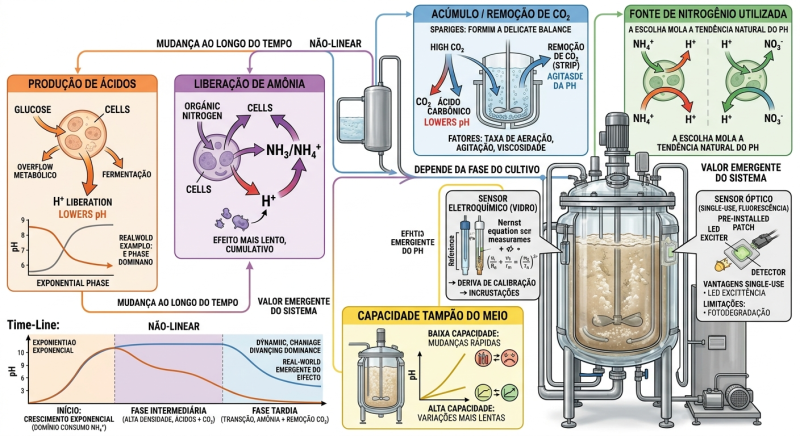
Em um biorreator, o pH é o resultado de um balanço dinâmico de geração e consumo de prótons (H⁺). Cada fator atua simultaneamente, muitas vezes em direções opostas. O valor medido é, portanto, uma variável emergente do sistema, não um efeito isolado.
Componentes que determinam o pH
Produção de ácidos
Origem:
- metabolismo celular (overflow, fermentação, subprodutos)
Efeito:
- Liberação de H⁺ → queda de pH
Intensidade depende de:
- Disponibilidade de substrato
- Limitação de oxigênio
- Tipo celular
- Liberação de amônia
Origem:
- Desaminação de aminoácidos
- Metabolismo de nitrogênio orgânico
Efeito:
NH₃/NH₄⁺ consome H⁺ → aumento de pH
Característica:
- Efeito mais lento, porém cumulativo
Acúmulo / remoção de CO₂
- CO₂ dissolvido forma ácido carbônico → reduz pH
- Remoção de CO₂ (strip) → elevação do pH
Fonte de nitrogênio utilizada
NH₄⁺ (amônio):
Consumo libera H⁺ → acidificação
NO₃⁻ (nitrato):
Redução intracelular consome H⁺ → alcalinização
→ A escolha da fonte de nitrogênio molda a tendência natural do pH
Capacidade tampão do meio
- Determina quanto o pH resiste à mudança
- Alta capacidade tampão:
- Variações mais lentas
Baixa capacidade:
- Mudanças rápidas e mais difíceis de controlar
Interação real (não linear)
Esses fatores:
- Não atuam de forma independente
- Não possuem efeito constante
- Mudam ao longo do tempo
→ O sistema é não linear e dependente da fase do cultivo
Exemplo real
- Início do cultivo (fase de crescimento exponencial)
Fenômenos dominantes:
- Alto consumo de nutrientes (principalmente NH₄⁺)
- Baixa produção de subprodutos
Efeito principal:
- Consumo de NH₄⁺ → liberação de H⁺
→ queda gradual do pH
Observação crítica:
- pH pode cair mesmo com células “saudáveis”
→ não é necessariamente um problema - Fase intermediária (alta densidade celular)
Interações:
- CO₂ também aumenta → reforça acidificação
- Tampão começa a ser consumido
Risco:
- Queda rápida → necessidade de intervenção
- Indica possível desbalanceamento do processo
- Fase tardia (transição para estacionária)
Efeito combinado:
- Liberação de amônia (degradação celular ou metabolismo)
Remoção mais eficiente de CO₂ (menor produção)
→ elevação do pH
Interpretação crítica dessa fase:
- Subida de pH pode indicar:
- Exaustão de substrato
- Mudança de metabolismo
- Início de declínio celular
→ Não é “melhora”, é mudança de estado do sistema
Interação dinâmica:
Ao longo do processo, o controle de pH enfrenta:
- Mudança na causa dominante:
- Início: consumo de NH₄⁺
- Meio: produção de ácidos
- Final: liberação de bases + remoção de CO₂
- Mudança na intensidade dos efeitos
- Mudança na capacidade tampão efetiva
Implicação para controle:
Um mesmo ajuste (ex: adição de base) pode ter efeitos diferentes dependendo da fase:
- No início: resposta previsível
- No meio: pode ser insuficiente
- No final: pode causar overshoot
Síntese técnica:
- O pH é determinado por múltiplos fatores simultâneos
- A dominância de cada fator muda ao longo do tempo
- O comportamento observado é resultado de:
- Interações metabólicas
- Transferência de massa
- Equilíbrios químicos
Métodos de medição de pH em biorreatores
A medição de pH em biorreatores exige alta confiabilidade, resposta rápida e estabilidade em condições severas (temperatura, pressão, esterilização, alta carga celular). Pequenos erros impactam diretamente o controle do processo.
Sensores eletroquímicos: Princípio de funcionamento
- Baseado na diferença de potencial elétrico entre:
- Eletrodo de medição (membrana de vidro sensível a H⁺)
- Eletrodo de referência (potencial constante)
- A voltagem gerada segue a equação de Nernst, proporcional ao pH.
Por que são os mais utilizados?
- Alta precisão (±0,01–0,05 pH)
- Resposta rápida
- Tecnologia consolidada e robusta
- Compatíveis com sistemas industriais (inclusive CIP/SIP)
Limitações reais (além do “desgaste”)
- Deriva ao longo do tempo:
- Envelhecimento da membrana de vidro
- Contaminação do eletrólito de referência
Sensibilidade à temperatura:
- Exige compensação automática (ATC)
- Erro em meios complexos:
- Alta força iônica
- Presença de proteínas e sólidos
Problemas típicos em operação
- Resposta mais lenta com o tempo
- Ruído no sinal
- Leituras inconsistentes em alta densidade celular
Sensores ópticos
Princípio de funcionamento
- Baseados em corantes sensíveis ao pH imobilizados em uma matriz
- O pH altera propriedades como:
- Intensidade de fluorescência
- Tempo de decaimento (lifetime)
- Medição feita por excitação óptica (LED) e leitura do sinal emitido
Vantagens operacionais
- Não dependem de corrente elétrica no meio → menos interferência eletroquímica
Menor impacto de:
- Ruído elétrico
- Gradientes de potencial
Podem ser usados em:
- Sistemas descartáveis (single-use)
Microbiorreatores: Limitações reais
- Menor precisão absoluta em comparação com eletrodos de vidro (em alguns casos)
- Fotodegradação do corante ao longo do tempo
Sensibilidade a:
- Temperatura
- Intensidade de luz
- Faixa de medição pode ser mais limitada dependendo do sensor
Tendência industrial
Crescente adoção em:
- Bioprocessos modernos
- Indústria farmacêutica (single-use)
- Especialmente úteis onde eletrodos tradicionais são difíceis de manter
Principais desafios na medição de pH
- Deriva de calibração
- O sensor perde acurácia gradualmente
- Causas:
- Envelhecimento
- Contaminação
- Condições severas de operação
Impacto real:
- Controle baseado em valores incorretos
- Adição excessiva de ácido/base
- Desvio silencioso do processo
Incrustações:
- Deposição de:
- Proteínas
- Biomassa
- Sais
- Forma uma barreira física sobre o sensor
Consequências:
- Resposta lenta
- Leituras “travadas” ou amortecidas
- Subestimação de variações reais de pH
- Necessidade de manutenção constante
Inclui:
- Calibração frequente (buffers padrão)
- Limpeza química ou mecânica
- Substituição periódica
Ponto crítico:
- Em processos longos (fed-batch, contínuos), a manutenção é limitada → risco acumulado de erro
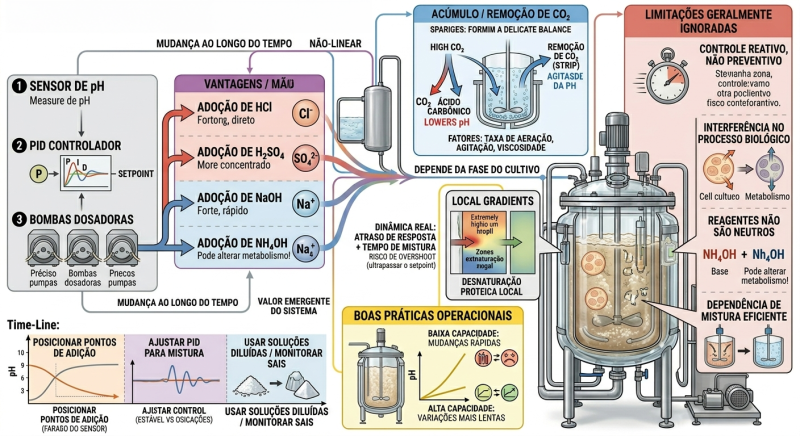
Estratégias de controle de pH - Controle por adição de ácido e base
Antes de entrar nas técnicas, é importante entender que nenhuma estratégia isolada garante resultado — o desempenho real vem de como o bioprocesso é controlado como um todo. Aprofunde essa lógica em: O que realmente garante resultados confiáveis em um biorreator não é o equipamento — é o controle de bioprocesso.
É o método mais direto e amplamente utilizado, mas também um dos mais mal interpretados quando aplicado sem considerar a dinâmica do processo.
Como funciona
- Correção direta com reagentes químicos
- Um sensor mede o pH em tempo real.
- Um controlador (geralmente PID) compara com o setpoint.
- Quando há desvio:
- Injeta-se ácido (para reduzir pH)
- Injeta-se base (para aumentar pH)
Elementos do sistema:
- Sensor de pH
- Controlador (PID ou on/off)
- Bombas dosadoras ou válvulas
- Tanques de ácido/base
Dinâmica real do sistema
- A correção não é instantânea e homogênea:
- Existe tempo de mistura
- Gradientes locais de pH podem ocorrer
O sistema responde com atraso → risco de overshoot (ultrapassar o setpoint)
Exemplos de reagentes:
- Ácidos
- HCl (ácido clorídrico)
- Forte, ação rápida
- Pode aumentar concentração de cloretos
- H₂SO₄ (ácido sulfúrico)
- Mais concentrado → menor volume necessário
- Pode impactar balanço de sulfatos
- Bases
- NaOH (hidróxido de sódio)
- Forte, resposta rápida
- Aumenta carga iônica e osmolaridade
- NH₄OH (hidróxido de amônio)
- Atua como base e fonte de nitrogênio
- Pode alterar metabolismo (não é neutro do ponto de vista biológico)
Vantagens:
- Simples implementação
- Alta capacidade de correção
- Fácil integração em sistemas industriais
- Baixo custo inicial
- Controle direto e intuitivo
- Funciona bem mesmo em processos com variações intensas de pH
Desvantagens:
- Oscilações bruscas
Causas:
- Resposta atrasada do sistema (sensor + mistura)
- Dosagem excessiva (controle mal ajustado)
- Controle on/off em vez de PID fino
Consequências:
- Flutuações de pH (instabilidade)
- Estresse celular
- Redução de produtividade
- Alteração da osmolaridade
Cada adição de ácido/base introduz íons no meio:
- HCl → Cl⁻
- NaOH → Na⁺
- H₂SO₄ → SO₄²⁻
Impacto real:
- Aumento da força iônica
- Alteração da pressão osmótica
- Pode causar:
- Estresse celular
- Redução de crescimento
- Mudança no metabolismo
Limitações que geralmente são ignoradas
Controle reativo, não preventivo
- Atua depois que o pH já desviou
- Não resolve a causa (metabolismo, CO₂, alimentação)
Interferência no processo biológico
- Reagentes não são “neutros”:
- NH₄OH altera balanço de nitrogênio
- NaOH pode inibir células sensíveis
Gradientes locais de pH
- Próximo ao ponto de adição:
- pH pode ser extremamente alto ou baixo momentaneamente
- Pode causar:
- Danos celulares localizados
- Desnaturação de proteínas
Dependência de mistura eficiente
- Sem boa agitação:
- Correção não se distribui corretamente
- Sensor pode não refletir o pH real do sistema
Boas práticas operacionais
- Posicionar ponto de adição longe do sensor
- Garantir alta eficiência de mistura
- Ajustar corretamente parâmetros do controlador (PID)
- Usar soluções diluídas para evitar choques locais
- Monitorar acúmulo de sais ao longo do processo
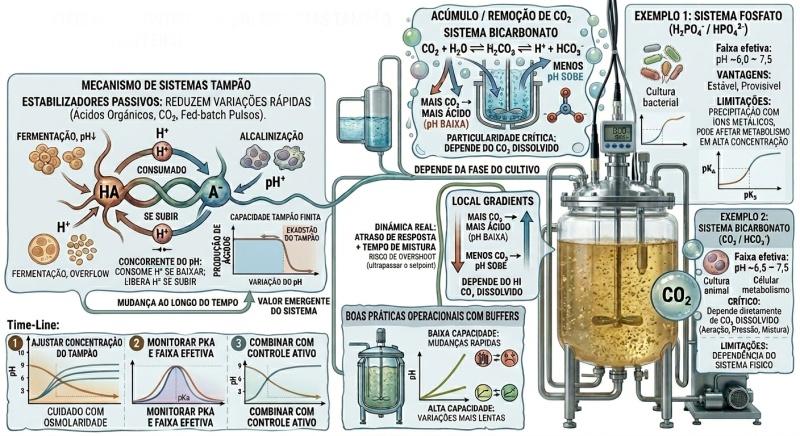
Uso de sistemas tampão (buffers)
Buffers são utilizados para amortecer variações de pH, tornando o sistema mais estável frente às perturbações metabólicas e operacionais. Diferente da adição direta de ácido/base, eles atuam de forma passiva e contínua.
Função:
- Reduz variações rápidas de pH
- Um sistema tampão é composto por:
- Um ácido fraco
- Sua base conjugada
- Ele atua consumindo ou liberando H⁺ conforme necessário:
- Se o meio acidifica → o tampão absorve H⁺
- Se o meio alcaliniza → o tampão libera H⁺
Mecanismo prático:
- Minimiza oscilações causadas por:
- Produção de ácidos orgânicos
- Variações na aeração (CO₂)
- Pulsos de alimentação (fed-batch)
Exemplos:
- Fosfatos (sistema fosfato: H₂PO₄⁻ / HPO₄²⁻)
Características:
- Faixa efetiva de atuação: pH ~6,0 – 7,5
- Muito utilizado em:
- Culturas bacterianas
- Meios laboratoriais e industriais
Vantagens:
- Boa capacidade tampão próximo ao pH neutro
- Relativamente estável e previsível
Limitações:
- Pode interagir com:
- Íons metálicos (precipitação)
- Em altas concentrações:
- Afeta metabolismo celular
- Bicarbonatos (sistema CO₂ / HCO₃⁻)
Equilíbrio químico:
CO₂ + H₂O ⇌ H₂CO₃ ⇌ H⁺ + HCO₃⁻
Características:
- Faixa efetiva: pH ~6,5 – 7,5
- Muito utilizado em:
- Cultura de células animais
Particularidade crítica:
- Depende diretamente do CO₂ dissolvido:
- Mais CO₂ → mais ácido → pH diminui
- Menos CO₂ → pH sobe
Implicação:
- pH não depende só do tampão, mas também de:
- Aeração
- Pressão
- Transferência de massa
Por quê?
- Cada sistema tampão tem uma capacidade tampão finita, definida por:
- Concentração do tampão
- Proximidade do pKa
O que acontece na prática:
- Com o tempo:
- Produção contínua de ácidos ou bases “consome” o tampão
- Quando esgota:
- pH passa a variar rapidamente
- Sistema perde estabilidade
Limitações adicionais (frequentemente ignoradas)
Faixa de atuação restrita
- Buffers funcionam melhor próximos ao seu pKa
- Fora dessa faixa:
- Eficiência cai drasticamente
Interferência no processo biológico
- Alta concentração de tampão pode:
- Alterar osmolaridade
- Inibir crescimento celular
- Interferir em vias metabólicas
Impacto em downstream
- Pode dificultar:
- Purificação
- Precipitação de produtos
- Especialmente relevante em processos farmacêuticos
Dependência do sistema físico (no caso do bicarbonato)
- Alterações em:
- Aeração
- Agitação
→ mudam o equilíbrio do tampão, afetando o pH indiretamente
Papel estratégico no controle de pH
Buffers não substituem o controle ativo, mas:
- Reduzem a carga do sistema de controle (menos adições de ácido/base)
- Melhoram estabilidade em:
- Processos sensíveis (células animais)
- Escalas pequenas (laboratório, desenvolvimento)
Síntese técnica
- Buffers atuam como estabilizadores passivos
- Eficientes contra variações rápidas e pequenas
- Limitados frente a perturbações prolongadas ou intensas
- Devem sr combinados com estratégias ativas de controle
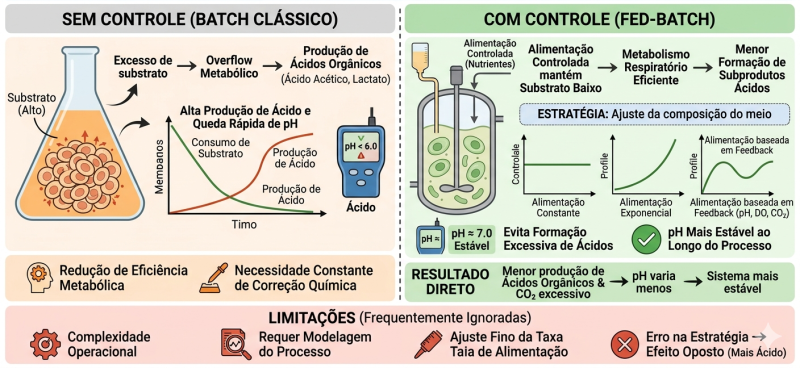
Controle por alimentação (fed-batch)
Essa estratégia atua de forma indireta e preventiva sobre o pH, ajustando o metabolismo celular em vez de apenas corrigir o desvio após ele ocorrer.
Estratégia:
- Ajuste da composição do meio
No modo fed-batch, nutrientes (principalmente carbono e nitrogênio) são adicionados de forma controlada ao longo do tempo, em vez de estarem todos disponíveis desde o início.
Objetivo central:
- Controlar a taxa metabólica das células
- Evitar excesso de substrato → evitar desequilíbrios metabólicos
Mecanismo chave (ponto crítico)
Quando há excesso de substrato (ex: glicose):
- As células entram em overflow metabólico
- Produzem subprodutos ácidos:
- Ácido acético (E. coli)
- Lactato (células animais)
Isso causa:
→ Queda de pH
→ Redução de eficiência metabólica
Como o fed-batch resolve isso:
- Alimentação controlada mantém o substrato em níveis baixos
- Força a célula a operar em metabolismo mais eficiente (respiratório)
- Reduz formação de subprodutos
Tipos de estratégia de alimentação
- Alimentação constante
- Alimentação exponencial
- Alimentação baseada em feedback
- Taxa fixa de adição
- Simples, mas pouco adaptativa
- Acompanha crescimento celular
- Mantém taxa específica de crescimento (μ) controlada
Ajustada com base em variáveis como:
- pH
- oxigênio dissolvido (DO)
- CO₂
Benefício:
- Evita formação excessiva de ácidos
Esse é o principal impacto sobre o pH
Por quê?
- Reduz fluxo metabólico desviado para vias fermentativas
- Mantém equilíbrio entre:
- Geração de energia
- Produção de biomassa/produto
Resultado direto:
- Menor produção de:
- Ácidos orgânicos
- CO₂ excessivo
- pH mais estável ao longo do processo
Sem controle (batch clássico):
- Substrato alto → produção de ácido → pH cai
- Necessidade constante de correção química
Com fed-batch:
- Substrato limitado → metabolismo controlado
- pH varia menos → sistema mais estável
Limitações (frequentemente ignoradas)
Complexidade operacional
Requer:
- Modelagem do processo
- Ajuste fino da taxa de alimentação
Erro na estratégia → efeito oposto (mais ácido)
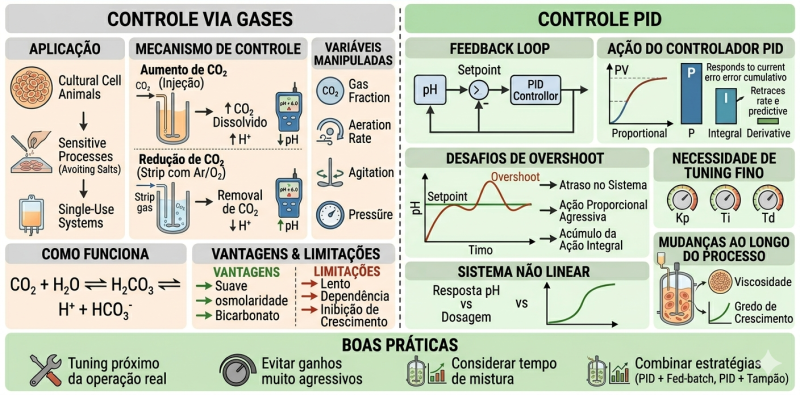
Controle via gases
Aplicação
- Muito usado em cultura celular
- Predominante em cultivos de células animais e alguns processos sensíveis, onde:
- Evita adição excessiva de sais (como Na⁺, Cl⁻)
- Mantém condições mais próximas do ambiente fisiológico
- Também aplicado em sistemas single-use, onde eletrodos e adições químicas são mais limitados
Como funciona:
- Ajuste da concentração de CO₂
Baseia-se no equilíbrio:
CO₂ + H₂O ⇌ H₂CO₃ ⇌ H⁺ + HCO₃⁻
Mecanismo de controle
- Aumento de CO₂ (injeção no gás):
- Mais CO₂ dissolvido → mais H⁺
→ pH diminui - Redução de CO₂ (strip com ar/O₂):
- Remoção de CO₂ → consumo de H⁺
→ pH aumenta
Variáveis manipuladas:
- Fração de CO₂ no gás de entrada
- Taxa de aeração
- Intensidade de agitação (impacta transferência de massa)
- Pressão do sistema
Vantagens:
- Não altera significativamente a osmolaridade
- Controle mais “suave” (menos choques químicos)
- Integra-se naturalmente com sistemas tampão bicarbonato
Limitações:
- Dependente da eficiência de transferência de massa
- Pode ser lento em grandes volumes
- Excesso de CO₂ dissolvido pode:
- Inibir crescimento celular
- Alterar metabolismo
Controle avançado de pH em biorreatores
Controle PID (Proporcional–Integral–Derivativo)
Características
- Automático e amplamente utilizado
- Sistema fechado (feedback loop):
- Mede pH
- Compara com setpoint
- Ajusta ação de controle
- Ajusta dosagem em tempo real
O controlador combina três ações:
- Proporcional (P):
- Responde ao erro atual (diferença entre pH medido e desejado)
- Quanto maior o erro → maior a correção
- Integral (I):
- Corrige erros acumulados ao longo do tempo
- Elimina desvios persistentes
- Derivativo (D):
- Reage à velocidade de mudança do pH
- Atua como “freio”, evitando excesso de correção
Onde o PID atua
- Dosagem de ácido/base
- Ajuste de CO₂
- Estratégias combinadas (multivariáveis)
Desafios
- Overshoot (ultrapassagem do setpoint)
Por que acontece:
- Atraso no sistema:
- Tempo de mistura
- Tempo de resposta do sensor
- Ação proporcional muito agressiva
- Acúmulo da ação integral
Consequências:
- Oscilações de pH
- Estresse celular
- Instabilidade no processo
- Necessidade de tuning fino
O que é tuning:
- Ajuste dos parâmetros:
- Ganho proporcional (Kp)
- Tempo integral (Ti)
- Tempo derivativo (Td)
Problema real:
- Cada processo tem dinâmica própria:
- Viscosidade
- Taxa metabólica
- Escala do reator
→ Não existe configuração universal
Dificuldades práticas:
- Mudanças ao longo do processo:
- Crescimento celular altera comportamento do sistema
- Interações com outras variáveis:
- Aeração
- Alimentação (fed-batch)
- Sensores com atraso ou ruído
Limitações frequentemente ignoradas
Sistema não linear
- Resposta do pH não é proporcional à dosagem
- Depende de:
- Capacidade tampão
- Estado metabólico
Controle isolado é insuficiente
- PID corrige o pH, mas:
- Não controla a causa (metabolismo, CO₂, nutrientes)
Interação entre variáveis
- Ajustar CO₂ pode afetar:
- Oxigênio dissolvido
- Crescimento celular
Boas práticas
- Fazer tuning em condições próximas da operação real
- Evitar ganhos muito agressivos
- Considerar tempo de mistura no ajuste
- Combinar estratégias:
- PID + fed-batch
- PID + tampão
- PID + controle de gases
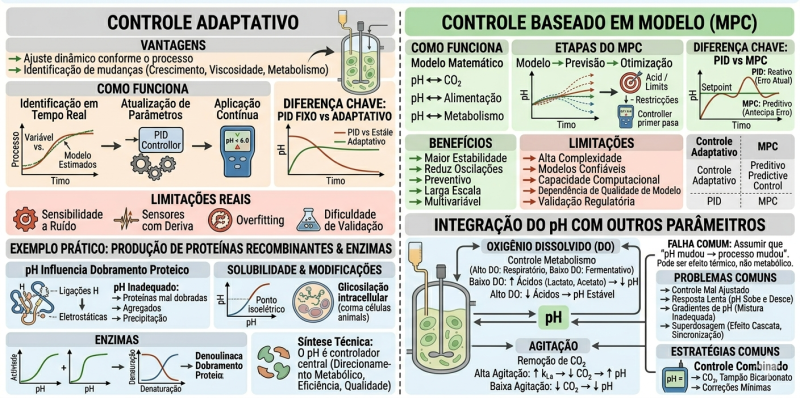
Controle adaptativo
Diferente do PID fixo, o controle adaptativo ajusta seus próprios parâmetros automaticamente conforme o comportamento do processo muda ao longo do tempo.
Vantagens
- Ajuste dinâmico conforme o processo
- O sistema identifica mudanças como:
- Crescimento celular (aumento de biomassa)
- Alteração na viscosidade
- Mudanças na taxa metabólica
- Recalibra parâmetros de controle (ex: ganhos do PID) em tempo real
Resultado:
- Mantém desempenho estável mesmo com dinâmica variável
- Ideal para sistemas não lineares
Biorreatores são naturalmente:
- Não lineares
- Dependentes do tempo
Relação entre:
- Adição de ácido/base
- Resposta de pH
→ muda ao longo do cultivo
O controle adaptativo consegue:
- Ajustar-se a essas mudanças
- Evitar perda de desempenho típica de controladores fixos
Como funciona:
Existem diferentes abordagens, mas geralmente envolvem:
- Identificação do sistema em tempo real
- Estima como o processo está respondendo naquele momento
- Atualização dos parâmetros de controle
- Ajusta automaticamente ganhos e tempos
- Aplicação contínua
- O controlador evolui junto com o processo
Limitações reais:
- Sensível a:
- Ruído de medição
- Sensores com deriva
- Pode reagir a “falsas mudanças” (overfitting do controle)
- Mais difícil de validar em ambientes regulados (ex: farmacêutico)
Controle baseado em modelo (MPC – Model Predictive Control)
Como funciona:
- Usa modelos matemáticos para prever comportamento
O MPC utiliza um modelo do processo para responder à pergunta:
“Se eu fizer essa ação agora, o que vai acontecer com o pH nos próximos minutos?”
Etapas do MPC
- Modelo do processo
- Representa relações como:
- pH ↔ CO₂
- pH ↔ alimentação
- pH ↔ metabolismo
Previsão:
- Simula o comportamento futuro do sistema em um horizonte de tempo
Otimização
- Calcula a melhor ação de controle considerando:
- Setpoint
- Restrições (ex: evitar excesso de ácido)
Ação:
- Aplica apenas o primeiro passo da estratégia
- Repete o ciclo continuamente
Diferença chave vs PID
- PID reage ao erro atual
- MPC antecipa o erro antes que ele aconteça
Benefícios:
- Maior estabilidade
Reduz oscilações porque:
- Atua de forma preventiva
- Considera atrasos do sistema (mistura, sensores)
- Melhor performance em larga escala
Em grandes biorreatores:
- Tempo de resposta é mais lento
- Não linearidades são mais fortes
O MPC consegue:
- Lidar melhor com essas limitações
- Coordenar múltiplas variáveis simultaneamente
Benefícios adicionais
Controle multivariável:
- Ajusta simultaneamente:
- pH
- CO₂
- alimentação
Respeita limites operacionais:
- Evita ações agressivas
- Reduz consumo de reagentes
Limitações
- Alta complexidade
Requer:
- Desenvolvimento de modelo confiável
- Conhecimento profundo do processo
- Modelos podem ficar obsoletos com mudanças no sistema
- Requer capacidade computacional
- Necessita resolver problemas de otimização em tempo real
Em sistemas rápidos ou grandes:
- Demanda processamento contínuo
Limitações adicionais (frequentemente ignoradas)
- Dependência da qualidade do modelo
- Integração difícil
- Validação regulatória
Modelo ruim → controle ruim (ou instável)
Precisa se comunicar com:
- Sensores
- Atuadores
- Sistema supervisório
Em indústrias como farmacêutica:
Mais difícil de validar que PID tradicional
|
Característica |
Controle Adaptativo |
MPC |
|
Base |
Ajuste de parâmetros |
Modelo Matemático |
|
Reação vs previsão |
Reativo Adaptativo |
Preditivo |
|
Complexidade |
Média |
Alta |
|
Robustez |
Boa |
Muito alta (se bem modelado) |
|
Aplicação típica |
Processos variáveis |
Processos críticos/escala |
Integração do pH com outros parâmetros do processo
O pH não é uma variável isolada. Ele está fortemente acoplado a fenômenos físico-químicos e metabólicos. Ajustar pH sem considerar essas interações leva a controle instável ou interpretações erradas do processo.
Falha comum
Assumir que:
“pH mudou → processo mudou”
Pode ser apenas efeito térmico, não metabólico.
Oxigênio dissolvido (DO)
Influencia metabolismo celular
DO controla o tipo de metabolismo:
- Alto DO → metabolismo respiratório
- Baixo DO → metabolismo fermentativo
Impacto direto no pH
Baixo DO:
- Aumento de subprodutos ácidos (ex: lactato, acetato)
→ pH cai
Alto DO:
- Menor formação de ácidos
→ pH mais estável
Interação crítica
- Ajustar DO (via aeração/agitação) altera:
- Produção de CO₂
- Formação de metabólitos
→ efeito indireto, mas forte sobre o pH
Agitação
- Impacta remoção de CO₂
- A agitação influencia o coeficiente de transferência de massa (kLa)
Efeito sobre o pH
- Alta agitação:
- Melhor remoção de CO₂
→ menor formação de ácido carbônico
→ pH tende a subir - Baixa agitação:
- Acúmulo de CO₂
→ pH tende a cair
→ O pH observado é um resultado combinado, não uma causa isolada.
Problemas comuns no controle de pH
• Controle mal ajustado
• Resposta lenta do sistema
Consequências:
- pH “sobe e desce” continuamente
- Estresse celular
- Perda de produtividade
Gradientes de pH
- Mistura inadequada
- Comum em grandes volumes
- Distribuição não uniforme de ácido/base ou CO₂
- Em biorreatores industriais:
- Pode haver zonas com pH diferente do valor medido
Efeito na medição:
- Resposta lenta
- Leituras amortecidas ou incorretas
Consequências:
- Controle baseado em dados errados
- Correções desnecessárias ou excessivas
Causas:
- Superdosagem de ácido/base
- Falta de sincronização com tempo de mistura
- Controle reativo sem considerar dinâmica
Efeito cascata:
- pH desvia
- Correção exagerada
- pH ultrapassa o setpoint
- Nova correção → ciclo contínuo
→ Pequenas variações podem comprometer o produto final
Estratégia comum
- Controle combinado:
- CO₂ (controle fino)
- Tampão bicarbonato
- Correções químicas mínimas
Estratégia comum
- Manter pH próximo ao:
- Ótimo de expressão durante cultivo
- Ótimo de estabilidade após secreção
Exemplo prático
- Produção de proteínas recombinantes
Contexto
- Produção em:
- E. coli, leveduras ou células animais
Por que o controle de pH é crítico?
Dobramento proteico (protein folding)
- pH influencia interações:
- Ligações de hidrogênio
- Interações eletrostáticas
→ pH inadequado:
- Gera proteínas mal dobradas
- Formação de agregados (inclusão)
Solubilidade da proteína:
- Depende do estado de carga da molécula
- pH próximo ao ponto isoelétrico:
- Aumenta risco de precipitação
Modificações pós-traducionais:
- Em células animais:
- Glicosilação depende do ambiente intracelular
- pH influencia essas vias indiretamente
Estabilidade do produto:
- Mesmo após secreção:
- pH pode degradar ou desnaturar a proteína
Consequência prática:
- pH fora da faixa:
- Produto perde atividade
- Pode se tornar inutilizável, mesmo que produzido em alta quantidade
Síntese técnica:
- O pH é um dos principais controladores de:
- Direcionamento metabólico
- Eficiência de produção
- Qualidade final
- Cada setor utiliza o pH de forma estratégica:
- Antibióticos → controle de fases metabólicas
- Fermentação → controle microbiológico
- Farmacêutico → controle de qualidade molecular
Enzimas → estabilidade e atividade
- Produção de enzimas
Características do processo:
- Pode envolver bactérias ou fungos
- Produto final é altamente sensível ao ambiente
Papel do pH
- Afeta:
- Expressão da enzima
- Estabilidade após produção
Impactos práticos:
- pH inadequado pode:
- Desnaturar a enzima
- Reduzir atividade catalítica
Conclusão
O controle de pH em biorreatores não é apenas uma variável operacional, mas um elemento estruturante do desempenho do processo, impactando simultaneamente metabolismo celular, rendimento e qualidade do produto. Sua relevância se amplia à medida que aumentam a complexidade biológica e a escala produtiva.
Estratégias convencionais, como adição de ácido/base e uso de tampões, continuam essenciais pela robustez e simplicidade, porém apresentam limitações quando aplicadas isoladamente. Abordagens mais avançadas — como controle por gases, estratégias fed-batch, controle adaptativo e controle preditivo baseado em modelo (MPC) — permitem uma atuação mais precisa, antecipativa e alinhada à dinâmica real do sistema.
A tendência consolidada aponta para a evolução de biorreatores em direção a sistemas cada vez mais automatizados, orientados por dados e preditivos, nos quais o pH deixa de ser apenas uma variável controlada e passa a ser um indicador-chave do estado metabólico e da estabilidade do processo.

